|
|||||
|
|||||||
|
    An initiative of :
|
|
Food-Info.net> Tematy > Barwniki żywności > Naturalne barwniki żywności Antocyjany i antocyjanidynyAntocyjany są dużą grupą czerwono-niebieskich barwników roślinnych. Występują w większości roślin wyższych, głównie w kwiatach i owocach, ale także w liściach, łodygach i korzeniach. Znajdują się przede wszystkim w zewnętrznych warstwach komórek. Zawartość antocyjanów jest dość duża; na przykład kilogram czarnych jagód zawiera ich około 1,15 g, a 1 g czerwonej i czarnej fasoli około 20 mg. Barwa antocyjanów zależy od ich budowy chemicznej, ale także od kwasowości owocu. Wiele antocyjanów ma czerwoną barwę w środowisku kwaśnym i zmienia ja na niebieską w mniej kwaśnym. Aglikony noszą nazwę antocyjanidyny, natomiast ich glikozydy to antocyjany. Są stosowane jako dodatki do żywności i oznaczone E163.
 Ryc. 1: Czarne jagody, bogate źródło antocyjanów (Źródło) StrukturaZ roślin wyizolowano ponad 500 różnych antocyjanów. W ich strukturze występuje pojedynczy, podstawowy rdzeń, tzw. jon flawyliowy (ryc. 2).
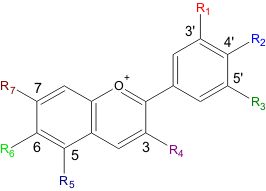 Ryc. 2 : Jon flawyliowy, podstawowa struktura antocyjanin. (Źródło) Z ryc. 2 wynika, że jon flawyliowy posiada 7 różnych bocznych grup chemicznych. Boczne grupy mogą stanowić atom wodoru, grupa wodorotlenowa lub metoksylowa. Najczęściej występujące kombinacje bocznych grup i ich nazwy przedstawiono w Tabeli 1. Tabela 1 : Główne grupy antocyjanidyn. R1-R7 są bocznymi grupami według ryc. 2.
Na podstawie literatury 2,3. Gdy antocyjanidyny łączą się z grupą cukrową, powstają antocyjany. Ponieważ grupa cukrowa może być przyłączona w różnych miejscach, a ponadto w roślinach występuje wiele różnych cukrów, oczywiste jest, że liczba powstałych antocyjanów może być bardzo duża. Na przykład do głównych antocyjanów w truskawkach należą dwa stosunkowo proste związki: 3-glukozyd cyjanidyny i 3-glukozyd pelargonidyny. Z kolei, w winogronach występują glukozydy cyjanidyny, pelargonidyny, petunidyny i malwidyny, a także di-glukozydy oraz niecukrowe antocyjanidyny. Należy dodać, że różnorodność związków barwnych zwiększa się, gdy uwzględnić możliwe kombinacje chemiczne cukrów z kwasami organicznymi (jak octowym, bursztynowym, kawowym i wieloma innymi), co w rezultacie tworzy antocyjany acetylowane. Przykładem takiego związku jest 3-acetyloglukozyd cyjanidyny w pomarańczach. Występowanie i funkcjeAntocyjany występują w niemal wszystkich rodzinach roślin, a zatem w wielu roślinach jadalnych. Wśród spożywanych produktów głównym źródłem antocyjanów są owoce jagodowe, jak jeżyny, winogrona, czarne jagody, itp., a także niektóre warzywa, jak bakłażan (oberżyna) i awokado. Do innych źródeł należą pomarańcza, czarny bez, oliwki, czerwona cebula, figi, słodkie ziemniaki, mango i fioletowa kukurydza. Oszacowano, że natura wytwarza 10 9 ton/rok antocyjanów. Tabela 2 : Zawartość antocyjanów w niektórych roślinach jadalnych
Antocyjany pełnią w roślinach szereg różnych funkcji. Są przeciwutleniaczami, chronią roślinę przed działaniem światła nadfioletowego i pełnią bardzo ważną rolę w zapylaniu i rozmnażaniu. Ponieważ antocyjany kształtują barwę wielu kwiatów, są także ważne w wabieniu owadów. Gatunki roślin zapylanych przez pszczoły, na przykład rodzina pierwiosnkowatych (Primulaceae), są bogate w antocyjany glukozydy delfinidyny, zaś inne antocyjany wabią bardziej trzmiele lub kolibry. Wykazano, że 3-glukozyd cyjanidyny należący do dość często spotykanych antocyjanów, chroni rośliny przed niektórymi larwami. Podobne działanie mogą wykazywać także inne antocyjany. Jako przeciwutleniacze, antocyjany chronią rośliny przed działaniem wolnych rodników (wytwarzanych pod wpływem światła słonecznego lub procesu niszczenia rośliny), które z kolei mogą uszkodzić DNA i doprowadzić do śmierci komórek. ZastosowanieAntocyjany są silnymi barwnikami rozpuszczalnymi w wodzie, od dawien dawna stosowanymi do barwienia żywności. Ekstrakty z różnych owoców jagodowych były stosowane do barwienia napojów, wypieków cukierniczych i innych produktów. Istnieją jednak pewne ograniczenia w zastosowaniu antocyjanów w produkcji żywności. Zastosowanie antocyjanów ogranicza ich rozpuszczalność w wodzie i pH środowiska. Gdy kwasowość zmienia się, zmienia się także ich barwa. Na przykład, barwa modrej kapusty staje się bardziej intensywna po dodaniu octu lub innego środka zakwaszającego. Z kolei, gdy kapustę gotuje się w naczyniu aluminiowym, w którym środowisko jest bardziej zasadowe, jej barwa zmienia się do fioletowej i niebieskiej. Barwa zależy także od temperatury, dostępu tlenu, działania światła nadfioletowego i innych czynników. Podwyższona temperatura może prowadzić do rozkładu jonu flawyliowego i w konsekwencji do zaniku barwy. Podwyższona temperatura może także skutkować reakcją Maillarda, w której mogą uczestniczyć reszty cukrowe antocyjanów. Podobne skutek może wywołać działanie światła. Z kolei, działanie tlenu może prowadzić do rozkładu antocyjanów, podobnie jak czynią to inne związki utleniające, np. nadtlenki i witamina C. Na antocyjany może oddziaływać szereg innych składników roślin i produktów żywnościowych i albo prowadzić do ich rozkładu, albo do zmiany barwy. Na przykład, chinony zawarte w jabłkach przyśpieszają rozkład antocyjanów, podczas gdy dodanie cukru do truskawek powoduje utrwalenie barwy. Wymienione czynniki ograniczają zastosowanie antocyjanów w produkcji żywności. Utracie barwy można zapobiegać stosując obniżoną temperaturę przechowywania, opakowania nieprzepuszczające światła lub pakowanie w atmosferze pozbawionej tlenu. W praktyce, trudno jest uzyskać czyste barwniki antocyjanowe i najczęściej do barwienia produktów spożywczych stosuje się surowe ekstrakty. Jako barwniki antocyjanowe wykorzystuje się głównie ekstrakt ze skórki winogron (E163(i)), oraz ekstrakt z czarnej porzeczki (E163(iii)). Aktywność i toksycznośćAntocyjany stosowane jako barwniki żywności nie są toksyczne, a ich stężenie w barwionych produktach nie przekracza wielkości, które spożywa się w owocach jagodowych lub innych owocach zawierających te barwniki. Toksyczność mocno skoncentrowanych mieszanin antocyjanów, oferowanych ostatnio jako suplementy żywieniowe, nie została jeszcze zbadana. Istnieją poglądy, że antocyjany mają cechy prozdrowotne, wynikające z ich właściwości przeciwutleniających. Dotyczy to obniżonej zapadalności na chorobę wieńcową, poprawy wzroku i aktywności antywirusowej. Wiele z tych poglądów nie jest jednak udowodnionych w badaniach naukowych. Choć antocyjany są ważnymi przeciwutleniaczami, ich wpływ na organizm człowieka jest wciąż słabo poznany.
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Food-Info.net is an initiative of Stichting Food-Info, The Netherlands | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||