|
|||||
|
|||||||
|
  
An initiative of :
Національний університет харчових технологій 
|
| Food-Info.net > Харчові інгредієнти > Білки АмінокислотиБілки є полімерами, побудованими з великої кількості амінокислот. Усього відомо 20 амінокислот, їх загальна хімічна формула RCH(NH2)COOH. Один атом азоту (N) та два атоми водню (H) складають аміногрупу (-NH2). Кислотні властивості молекули забезпечуються карбоксильною групою (-COOH). Радикал R- являє собою боковий ланцюг, будова якого, власно, і визначає амінокислоту. Лише одна амінокислота, пролін, має дещо іншу будову (див. табл. 1 нижче). Амінокислоти приєднуються одна до одної, завдяки тому, що карбоксильна група однієї молекули реагує з аміногрупою іншої з утворенням пептидного зв'язку (-C(=O) NH-) і виділенням молекули води (H2O). Пептид є сполукою двох чи більше амінокислот. Олігопептиди містять до 10 залишків амінокислот. Поліпептиди та білки є полімерами, що складаються з більше, ніж 10 молекул амінокислот, однак поліпептиди, що містять більше 50 залишків амінокислот, класифікують як білки.
* Незамінні амінокислоти
Термін «незамінні амінокислоти» стосується амінокислот, що беруть участь у фізіологічних процесах, але не синтезуються в організмі та мають надходити з їжею. Аргінін синтезується в організмі людини, проте лише у невеликих кількостях, що не задовольняють фізіологічну потребу у період росту. Метіонін потрібний у великих кількостях для того, щоб у разі нестачі у харчуванні цистеїну ця амінокислота утворювалася як похідна метіоніну. Подібним чином фенілаланін перетворюється на тирозин, і у разі дефіциту тирозину у раціоні фенілаланін має надходити до організму у великих кількостях. Тирозин є незамінною амінокислотою для хворих на фенілкетонурію ( PKU ) , в організмі яких фенілаланін не перетворюється на тирозин. Ізолейцин, лейцин і валін іноді називають «амінокислотами з розгалуженим ланцюгом», оскільки їх вуглецеві ланцюги мають розгалужену будову СтереохіміяВ усіх двадцяти амінокислотах, за винятком гліцину, атом вуглецю при аміногрупі зв'язаний з чотирма різними замісниками. Тетраедрична форма зв'язків вуглецю та асиметрія приєднаних груп зумовлюють наявність двох просторових ізомерів амінокислот ( L - і D - форми молекули ) , що є дзеркальним відображенням один одного (як права та ліва руки). У складі білків знайдено лише L- амінокислоти. У таких амінокислотах, якщо карбоксильну групу показати зверху, як на рисунку нижче, аміногрупа розташована зліва. Для просторового уявлення зв'язки, показані конусами, розташовані над площиною рисунку, а пунктирні зв'язки – під нею.
Структура пептиду, що складається з двох амінокислот
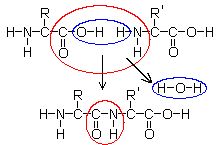
Цей рисунок показує взаємодію двох амінокислот. Літерами R і R ' позначені функціональні групи амінокислот (у табл. 1 вони наведені червоним кольором). Синім колом показано вивільнення молекули води (H2O) , а червоним – утворення пептидного зв'язку (-C(=O) NH-). Зворотна реакція, тобто руйнування пептидного зв'язку з утворенням вихідних амінокислот здійснюється у результаті гідролізу . У виробництві багатьох харчових продуктів використовуються смакові та ароматичні добавки, які отримують гідролізом рослинних білків. Соєвий соус отримують гідролізом суміші соєвих і пшеничних білків під час бродіння з використанням грибів роду Аspergillus або під час варіння у розчинах кислот. Глютамат натрію (MSG), підсилювач смаку, є натрієвою сіллю глютамінової кислоти. Ця сіль є складовою морських водоростей і соєвих продуктів, отриманих бродінням. Джерела :
|
|
| ||||||||||||||||||||||||||
| Food-Info.net is an initiative of Stichting Food-Info, The Netherlands | ||||||||||||||||||||||||||||||