|
|||||
|
|||||||
|
   
Een initiatief van :Stichting Food-Info
|
|
Food-Info.net> Onderwerpen > Ingrediënten > Kleurstoffen > Natuurlijke kleurstoffen Anthocyanen en anthocyanidinenDe anthocyanen vormen een zeer grote groep van kleurstoffen in rood-blauwe planten. Anthocyanen komen voor in allerlei hogere planten, vooral als kleurstof in bloemen en vruchten, maar ook in andere onderdelen van de plant, zelfs in wortels. In de stengels, bladeren en wortels komen ze echter meestal alleen voor in de buitenste lagen van de plant. Anthocyanen komen in vrij hoge concentraties voor; een kilo bosbessen bijvoorbeeld bevat ongeveer 1,15 gram, rode groenten, zoals rode kool, bevatten ongeveer 20 mg/gram aan anthocyanen. De kleur van anthicyanen hangt af van de structuur, maar ook van de zuurgraad van de plant. De meeste anthocyanen zijn rood bij zure condities en blauw/paars bij meer basische condities. Chemisch wordt er onderscheid ghemaakt tussen de suiker-vrije anthocyanidinen en de suiker-houdende anthocyaan-glycosiden. Anthocyanen worden als kleurstof gebruikt in levensmiddelen en hebben E-nummer E163.
 Fig. 1: Bosbessen, een rijke bron van anthocyanen (Bron) StructuurMeer dan 500 verschillende anthocyanen zijn uit planten geïsoleerd. Ze zijn echter allemaal afgeleid van één en dezelfde basisstructuur, het flavyllium ion (zie fuguur 2).
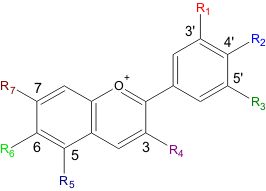 Fig. 2 : Het flavyllium ion, de basis voor alle anthocyanen. (Bron) Zoals in de bovenstaande structuur te zien is, zijn er 7 mogelijke zijgroepen aan dit flavyllium ion. Deze zijgroepen kunnen een waterstofatoom, een hydroxide-groep of een methoxy-groep zijn. De meest voorkomende combinaties van zijgroepen en de namen van de bijbehorende anthocyanindinen staan hieronder aangegeven. Tabel 1 : De belangrijkste anthocyanidinen. R1-R7 verwijzen naar de zijgroepen van figuur 2
Anthocyanen worden gevormd wanneer de anthocyanidinen gekoppeld worden aan suikers. Aangezien de suikers op verschillende plaatsen aan de anthocyanidinen gekoppeld kunnen worden, én er heel veel soorten suiekrs in planten voorkomen, is het logisch dat er een zeer grote hoeveelheid anthocyanen bestaan. Als voorbeeld; in aardbeien zijn de voornaamste anthocyanen cyanindine-3-glucoside en pelargonidine-3-glucoside, twee redelijk simpele structuren. In druiven, daarentegen, komen cyanidin-, pelargonidine-, delphinidine-, petunidine- en malvidine-glucosides en di-glucosides, evenals de vrije anthocyanindinen voor. Een nog grotere varieteit aan kleuren en structuren wordt veroorzaakt doordat aan de suiker-residuen weer zuren (zoals azijnzuur, barnsteenzuur, koffiezuur en andere zuren) gekoppeld kunnen worden. Een voorbeeld van zo'n geacectyleerde anthocyanine is cyanidine-3-(acetylglucoside) in sinaasappels. Voorkomen en functiesAangezien anthocyanen in vrijwel alle plantenfamilies kunnen worden aangetroffen, komen ze ook voor in vele eetbare planten. De belangrijktse bronnen van anthocyanen in ons voedsel zijn bessen, zoals bramen, druiven, bosbessen enz., maar ook sommige groentes, zoals aubergine en avocado. Andere belangrijke bronnen zijn sinaasappels, vlierbessen, olijven, rode uien, vijgen, zoete aardappelen, mango's en rode kool. De hoeveelheid anthocyanen die jaarlijks in de natuur worden geproduceerd wordt geschat op meer dan 1 miljard ton ! Tabel 2 : Anthocyaangehalte in eetbare planten
Anthocyanen hebben diverse functies voor de plant. Ze fungeren als anti-oxidanten, beschermen de plant tegen de schadelijke effecten van UV-straling, ze vormen een bescherming tegen insecten, maar de voornaamste rol is bij de voortplanting. De kleur van vele bloemen wordt veroorzaakt door anthocyanen en de kelur speelt een belangrijke rol om insecten aan te trekken. Planten die door bijen worden bevrucht , zoals primula's, hebben bijvoorbeeld meer delphinidine-anthocyanen, terwijl andere anthocyanen meer hommels of kolibries aantrekken. Cyaninidine-3-glucoside, een veel voornomende anthocyaan, beschermt bijvoorbeeld tegen diverse larven. Andere anthocyanen hebben vergelijkbare activiteit. Als anti-oxidant beschermen anthocyanen de plant tegen vrije radicalen (die door zonlicht of beschadiging worden gevormd), die het DNA kunnen beschadigen en zo het weefsel kunnen beschadigen. GebruikAnthocyanen zijn goed water oplosbaar, hebben een sterke kleur en worden daardoor al sinds historische tijden gebruikt als levensmiddelenkleurstof. Extracten van bessen werden bijvoorbeeld gebruikt om dranken, banket en andere levensmiddelen te kleuren. Er zitten echter een aantal nadelen aan het gebruik van anthocyanen in levensmiddelen. Het feit dat ze alleen oplosbaar zijn in water beperkt de toepassing. Een ander nadeel is de kleurverandering onder invloed van zuur. De kleur van rode kool wordt sterker als je er zuur (azijnzuur, appel) aan toevoegt. Als de kool daarentegen in een aluminium pan wordt gekookt wordt de kleur meer blauw-paars, doordat de pan het kookwater meer basisch maakt. De kleur is ook gevoelig voor tempertauur, zuurstof, UV-straling en diverse andere factoren. Het flavyllium ion is niet goed bestand tegen hitte en de kleur kan dan ook verloren gaan bij hogere temperaturen. De suikers van de anthocyanen kunnen bij verhitten ook reageren volgens de Maillard reacties, waarbij de kleur verloren gaat. Licht en UV straling breken de anthocyanen af, waardoor de kleur verloren gaat. Zuurstof en andere oxiderende stoffen, zoals peroxides en vitamine C kunnen ook met anthocyanen reageren. Ook andere componenten in levensmiddelen kunnen een effect hebben op de anthocyanen. Appels bevatten bijvoorbeeld quinonen die de afbraak van anthocyanen bevorderen, terwijl de suiker in aardbeien de kleur juist versterkt. Al dit soort factoren beperken de toepassing van anthocyanen. Door producten bij lage temperatuur en in een donkere, luchtdichte verpakking te bewaren kan kleurverlies grotendeels worden voorkomen. De meeste anthocyanen zijn niet of nauwelijks in zuivere vorm te verkrijgen. In de meeste gevallen worden dus extracten gebruikt als levensmiddelenkleurstof, de meest gebruikte zijn druivenschilextract (E163(i)) en zwarte bessen extract (E163(iii)). Activiteit en veiligheidAnthocyanen zijn niet giftig. De hoeveelheden die gebruikt worden als levensmiddelenkleurstof zijn veel lager dan de hoeveelheden die voorkomen in bessen of ander fruit. Er zijn echter ook voedingssupplementen in de handel met zeer hoge concentraties anthocyanen, de veiligheid van dergelijke hoge doseringen is niet verder onderzocht. Dergelijke supplementen zijn in de handel, omdat de anti-oxidant activiteit van anthocyanen een gezondheidsbevorderend effect zou hebben. Geclaimd worden een verlaagde kans op hart- en vaatziekten, verbeterde oogfunctie en anti-virale activiteit. Echter, deze claims zijn niet wetenschappelijk bewezen. Anthocyanen hebben wel degelijk anti-oxidant werking in het lichaam, maar de effecten op de menselijke gezondheid zijn eigenlijk nog onbekend.
|
|
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Food-Info.net is an initiative of Stichting Food-Info, The Netherlands | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||