|
|||||
|
|||||||
|
    An initiative of :Stichting Food-Info
|
| Food-Info.net > Θέματα > Δομικές μονάδες των τροφίμων > Πρωτεϊνες Πρωτεΐνες του γάλακτοςΤο γάλα περιέχει εκατοντάδες είδη πρωτεϊνών, τις περισσότερες σε πολύ μικρές ποσότητες. Οι πρωτεΐνες μπορούν να ταξινομηθούν με διάφορους τρόπους ανάλογα με τις χημικές ή φυσικές τους ιδιότητες και τις βιολογικές τους λειτουργίες. Παραδοσιακά οι πρωτεΐνες του γάλακτος διακρίνονταν στις καζεΐνες, τις πρωτεΐνες του ορού του γάλακτος και τις δευτερεύοντες πρωτεΐνες. Οι πρωτεΐνες που απαντούν στην επιφάνεια των λιποσφαιρίων και τα ένζυμα ανήκουν στην ομάδα των δευτερευόντων πρωτεϊνών.

Οι πρωτεΐνες του ορού του γάλακτος είναι ένας όρος που χρησιμοποιείται συχνά ως συνώνυμο των πρωτεϊνών του τυρογάλακτος, αλλά η χρήση του δεν πρέπει να περιλαμβάνει τις πρωτεΐνες του ορού του γάλακτος (τυρόγαλα) που παράγεται κατά την παρασκευή τυριού. Ο λόγος είναι ότι οι πρωτεΐνες του τυρογάλακτος περιέχουν πέρα από τις πρωτεΐνες του ορού του γάλακτος και κομμάτια των μορίων των καζεϊνών τα οποία οφείλονται στην δράση του ενζύμου ρεννίνη (πυτιά) στο γάλα της τυροκόμησης. Επίσης το τυρόγαλα περιέχει ορισμένες από τις πρωτεΐνες του ορού του γάλακτος σε μικρότερες συγκεντρώσεις από εκείνες που απαντούν στο γάλα εξαιτίας μετουσίωσης μέρους αυτών κατά την παστερίωση του γάλακτος που λαμβάνει χώρα πριν την τυροκόμηση. Οι τρεις αυτές κύριες ομάδες των πρωτεϊνών του γάλακτος διακρίνονται βάση της διαφορετικής τους συμπεριφοράς και μορφής. Οι καζεΐνες καθιζάνουν εύκολα κατά την επεξεργασία του γάλακτος με το ένζυμο ρεννίνη ή σε χαμηλό pH, ενώ οι πρωτεΐνες του ορού του γάλακτος παραμένουν συνήθως διαλυτές. Οι σφαιρικές πρωτεΐνες του ορού μετουσιώνονται κατά την ήπια θέρμανση του γάλακτος ενώ οι καζεΐνες παραμένουν σταθερές. Οι πρωτεΐνες της μεμβράνης των λιποσφαιρίων είναι προσκολλημένες στην επιφάνεια των λιποσφαιρίων και απελευθερώνονται μόνο κατά την εφαρμογή μηχανικής δύναμης, όπως π.χ. κατά την απόδαρση της κρέμας του γάλακτος για την παραγωγή βουτύρου.

ΚαζεΐνηΗ καζεΐνη είναι ένα όνομα που αναφέρεται στην κυρίαρχη ομάδα πρωτεϊνών του γάλακτος, τις καζεΐνες. Οι καζεΐνες υπάρχουν σε όλα τα γάλατα ζωικής προέλευσης, συμπεριλαμβανομένου και του ανθρώπινου. Στο αγελαδινό γάλα περίπου 80% των πρωτεϊνών είναι καζεΐνες (26 γραμμάρια ανά λίτρο γάλακτος). Οι καζεΐνες διακρίνονται σε τέσσερις υποομάδες: τις αs-,αs2-, β- και κ-καζεΐνες. Οι τέσσερις αυτές υποομάδες είναι πολύ ετερογενείς και περιλαμβάνει η καθεμιά 2-8 διαφορετικές γενετικές παραλλαγές. Αυτές οι παραλλαγές διαφέρουν μόνο σε ένα πολύ μικρό αριθμό αμινοξέων. Οι α- και β- καζεΐνες έχουν την ομοιότητα ότι τα αμινοξέα τους εστεροποιούνται σε φωσφορικό οξύ. Αυτό το φωσφορικό οξύ δένεται με το ασβέστιο (το οποίο υπάρχει σε αφθονία στο γάλα) σχηματίζοντας δεσμούς μεταξύ και εντός μορίων. Έτσι καθίσταται δυνατή η δημιουργία πολυμερών καζεϊνών που να περιέχουν αρκετά πανομοιότυπα ή διαφορετικά είδη καζεϊνών. Εξαιτίας της αφθονίας φωσφορικών ομάδων και υδρόφοβων περιοχών στο καζεϊνικό μόριο, τα πολυμερή των καζεϊνών είναι πολύ ιδιόμορφα και σταθερά. Τα πολυμερή αυτά αποτελούνται από εκατοντάδες ως χιλιάδες μόρια και σχηματίζουν ένα κολλοειδές διάλυμα στο οποίο οφείλεται το λευκό χρώμα του γάλακτος. Αυτά τα μοριακά σύμπλοκα είναι γνωστά ως καζεϊνικά μικκύλια. Τα καζεϊνικά μικκύλια, όπως φαίνεται στο σχήμα 1, αποτελούνται από ένα σύμπλοκο υπομικκυλίων, διαμέτρου 10 έως 15 nm (1 nm = 10-9 μέτρα). Ένα μικκύλιο μεσαίου μεγέθους αποτελείται από περίπου 400 με 500 υπομικκύλια και μπορεί να φθάσει σε μήκος τα 0.4 μm (0.0004 χιλιοστά).
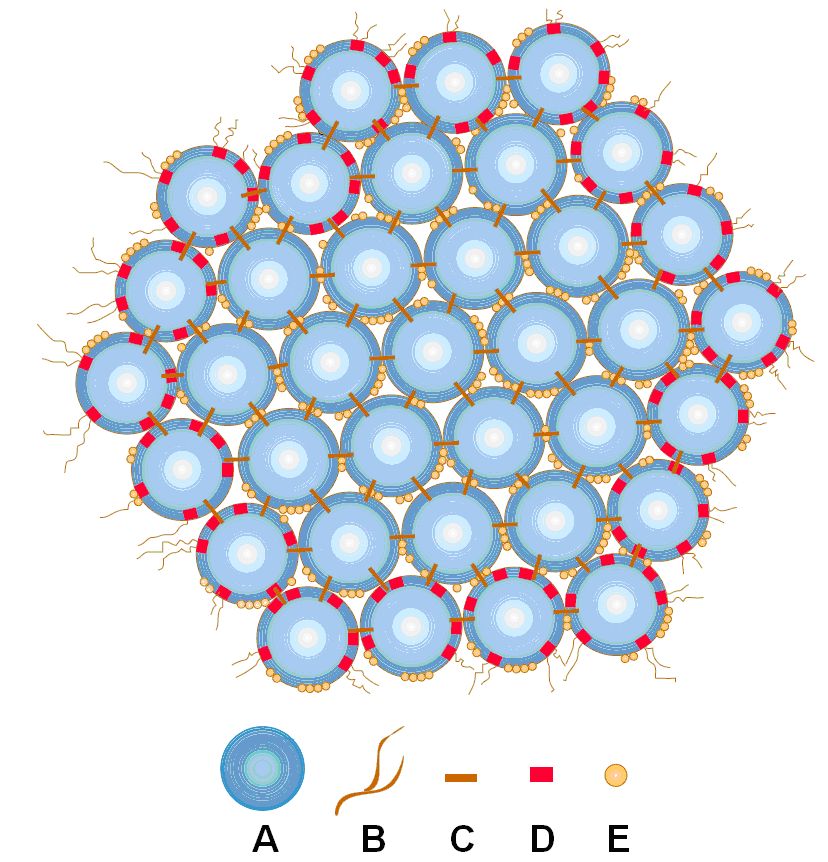 Σχήμα XX 1 Επάνω: Ένα καζεϊνικό μικκύλιο; Στη λεζάντα : A : ένα υπομικκύλιο. B : προεξέχουσα αλυσίδα. C : Φωσφορικό ασβέστιο. D : κ kappa -καζεΐνη. E : φωσφορικές ομάδες Το φωσφορικό ασβέστιο και οι υδρόφοβες αλληλεπιδράσεις μεταξύ των υπομικκυλίων είναι υπεύθυνες για την σταθερότητα των καζεϊνικών μικκυλίων. Τα υδρόφιλα τμήματα της κ-καζεΐνης περιέχουν ομάδες υδατανθράκων, οι οποίες προεξέχουν στην εξωτερική επιφάνεια των συμπλόκων των μικκυλίων (Β στο σχήμα 1), δίνοντας τους μία «τριχωτή» εμφάνιση και εμποδίζοντας την συσσωμάτωση τους. Η σπουδαιότητα της κ-καζεΐνης και των ομάδων υδατανθράκων της γίνεται φανερή κατά την παρασκευή τυριού. Η ρεννίνη που χρησιμοποιείται στο πρώτο στάδιο της τυροκόμησης, διασπά τον υδατάνθρακα από το μόριο της κ-καζεΐνης στην επιφάνεια των μικκυλίων. Αυτό έχει ως αποτέλεσμα τα μικκύλια να παύουν να είναι διαλυτά και να αρχίζουν να συσσωματώνονται σχηματίζοντας το τυρόπηγμα. Σε χαμηλή θερμοκρασία η δομή του μικκυλίου αποδυναμώνεται καθώς οι αλυσίδες της κ-καζεΐνης αρχίζουν να αποσυνδέονται και το υδροξυφωσφορικό ασβέστιο αφήνει το μικκύλιο. Η εξήγηση αυτού του φαινομένου έγκειται στο ότι η β-καζεΐνη είναι η πιο υδρόφοβη καζεΐνη και στο ότι οι υδρόφοβες αλληλεπιδράσεις αποδυναμώνονται με την μείωση της θερμοκρασίας. Η υδρόλυση της β-καζεΐνης σε γ-καζεΐνη και σε πρωτεόζες-πεπτόνες (προϊόντα διάσπασης) σημαίνει χαμηλότερη απόδοση σε τυρόπηγμα κατά την παρασκευή τυριού γιατί τα κλάσματα των πρωτεοζών-πεπτονών χάνονται στο τυρόγαλα. Η χρήση άλλων πρωτεολυτικών ενζύμων είναι επίσης δυνατή για την παρασκευή τυροπήγματος αλλά συχνά η δράση αυτών δεν είναι εξειδικευμένη. Τυρί το οποίο είναι παρασκευασμένο χωρίς τη χρήση ρεννίνης, με φυτικής προέλευσης πρωτεάσες (για χορτοφάγους), έχει συχνά διαφορετική γεύση ενώ η απόδοση σε τυρόπηγμα κατά την παρασκευή του είναι μειωμένη. Καθίζηση σε όξινο περιβάλλον Το φυσιολογικό pH του γάλακτος (6.5-6.7) είναι δυνατό να μειωθεί με την προσθήκη οξέων ή με την ανάπτυξη σε αυτό βακτηρίων που παράγουν οργανικά οξέα. Κατά την οξίνιση του γάλακτος οι ακόλουθες διεργασίες λαμβάνουν χώρα:
Οι δυο αυτές διεργασίες που λαμβάνουν χώρα κατά την παρασκευή τυριού, συνεπάγονται την αλλαγή των μικκυλίων τα οποία συσσωματώνονται και καταλήγουν τελικά στο σχηματισμό ενός λίγο ή πολύ πυκνού πήγματος. Σε προϊόντα ζύμωσης του γάλακτος όπως το γιαούρτι, βακτήρια επίσης παράγουν πολυσακχαρίτες οι οποίοι προσδίδουν κρεμώδη υφή στο σχηματιζόμενο πήγμα. Η καζεΐνη που έχει καθιζήσει είναι δυνατό να ξαναδιαλυθεί με την προσθήκη περίσσειας καυστικού νατρίου. Το σχηματιζόμενο κατά αυτό τον τρόπο καζεϊνικό νάτριο χρησιμοποιείται ως συστατικό των τροφίμων εξαιτίας των εξαιρετικών ιδιοτήτων του ως γαλακτωματοποιητής. Η αρχική δομή των μικκυλίων δεν μπορεί να αποκατασταθεί με την προσθήκη του καυστικού νατρίου.
 Διαχωρισμός του τυροπήγματος από το τυρόγαλα
Πρωτεΐνες τυρογάλακτοςΟι πρωτεΐνες του τυρογάλακτος είναι ένας όρος που συχνά χρησιμοποιείται για τις πρωτεΐνες του ορού του γάλακτος, αλλά τεχνικά περιλαμβάνει μόνο τις πρωτεΐνες εκείνες που είναι παρούσες στο τυρόγαλα το οποίο προκύπτει κατά την διαδικασία παρασκευής τυριού. Όταν η καζεΐνη απομακρυνθεί από το αποβουτυρωμένο γάλα με την επίδραση ανόργανων οξέων, αυτό που απομένει είναι ένα διάλυμα της ομάδας των πρωτεϊνών του ορού του γάλακτος. Αυτές οι πρωτεΐνες είναι πολύ όμοιες με τις πρωτεΐνες του τυρογάλακτος για αυτό το λόγο και συχνά οι δυο όροι συγχέονται. Οι πρωτεΐνες του ορού του γάλακτος αποτελούν περίπου το 20% του πρωτεϊνικού κλάσματος του γάλακτος. Οι πρωτεΐνες της ομάδας αυτής είναι πολύ διαλυτές και διακρίνονται στις ακόλουθες κατηγορίες:
Οι πρωτεΐνες του ορού του γάλακτος γενικά, και συγκεκριμένα η α-λακταλβουμίνη έχουν υψηλή βιολογική αξία. Η σύνθεση των αμινοξέων τους είναι πολύ κοντά σε αυτή που θεωρείται ως βέλτιστη από άποψη βιολογικής αξίας. Παράγωγα του ορού του γάλακτος χρησιμοποιούνται ευρέως στη βιομηχανία τροφίμων. Οι πρωτεΐνες του ορού μετουσιώνονται κατά την θέρμανση με συνέπεια τη συσσωμάτωση τους κυρίως με τα καζεϊνικά μικκύλια. Οι πρωτεΐνες του ορού του γάλακτος σε βιομηχανική κλίμακα απομονώνονται με τεχνολογίες μεμβρανών. α-λακταλβουμίνηΑυτή η πρωτεΐνη μπορεί να θεωρηθεί ως η χαρακτηριστική πρωτεΐνη του ορού του γάλακτος. Απαντά στο γάλα όλων των θηλαστικών και παίζει σημαντικό ρόλο στην σύνθεση της λακτόζης (γαλακτοσάκχαρο). β-λακτογλοβουλίνηΗ πρωτεΐνη αυτή απαντά μόνο στα οπληφόρα ζώα και είναι η κύρια πρωτεΐνη του ορού του γάλακτος των αγελάδων. Με την θέρμανση του γάλακτος στους 60 °C, ξεκινά η μετουσίωση των πρωτεϊνών του κατά την οποία η αντίδραση των θειούχων αμινοξέων της β-λακτογλοβουλίνης παίζει εξέχοντα ρόλο. Σε υψηλές θερμοκρασίες ελευθερώνονται θειούχες ενώσεις οι οποίες είναι κατεξοχήν υπεύθυνες για την οσμή και γεύση του θερμασμένου γάλακτος. ΑνοσοσφαιρίνεςΟι ανοσοσφαιρίνες παίζουν σημαντικό ρόλο στην προστασία του νεογγένητου ζώου (ή ανθρώπινου βρέφους) ενάντια σε βακτήρια και ασθένειες. ΛακτοφερίνηΗ λακτοφερίνη είναι μία γλυκοπρωτεΐνη που ανήκει στους μεταφορείς σιδήρου της οικογένειας των τρανσφερινών. Αρχικά απομονώθηκε από το βόειο γάλα αλλά απαντά και στο γάλα άλλων ζώων. Επιπροσθέτως, βρίσκεται και στις εξωκρινείς εκκρίσεις των θηλαστικών πέρα από το γάλα. Η λακτοφερίνη θεωρείται ως πολυλειτουργική πρωτεΐνη καθώς φαίνεται ότι έχει διάφορους βιολογικούς ρόλους. Εξαιτίας της ικανότητας της να δεσμεύει το σίδηρο, πιστεύεται ότι παίζει ρόλο στην απορρόφηση του σιδήρου από το βλεννογόνο του εντέρου των θηλαζόντων βρεφών. . Επίσης φαίνεται ότι έχει αντιβακτηριακή, αντιιική, αντιμυκητιακή, αντιφλεγμονώδη, αντιοξειδωτική και ανοσορυθμιστική δράση. Αυτές οι δραστηριότητες της μελετώνται εκτενώς. Για μία επισκόπηση των τρεχόντων μελετών δες http://www.lactoferrinresearch.org. ΛακτοπεροξειδάσηΗ λακτοπεροξειδάση έχει αναγνωριστεί ως αντιμικροβιακός παράγοντας στο γάλα, το σάλιο και τα δάκρυα. Πρόκειται για ένα φυσικό σύστημα άμυνας εναντίον των βακτηρίων μέσω της οξείδωσης των θειοκυανικών ιόντων (SCN-) από το υπεροξείδιο του υδρογόνου. Τα τελευταία είναι και τα δύο παρόντα στα βιολογικά υγρά και μαζί με τη λακτοπεροξειδάση αποτελούν το σύστημα της λακτοπεροξειδάσης (LP-s). Το LP-s έχει αποδειχθεί βακτηριοκτόνο ή βακτηριοστατικό σε μία ευρεία ποικιλία μικροοργανισμών, χωρίς να επιδρά στις πρωτεΐνες και τα ένζυμα των μικροοργανισμών που το παράγουν. Δευτερεύοντες ΠρωτεΐνεςΠρωτεΐνες των μεμβρανώνΟι πρωτεΐνες των μεμβρανών είναι μία ομάδα πρωτεϊνών που σχηματίζουν ένα προστατευτικό στρώμα γύρω από τα λιποσφαίρια με συνέπεια τη σταθεροποίηση του γαλακτώματος των σταγονιδίων λίπους στο γάλα. Ορισμένες από τις πρωτεΐνες αυτές περιέχουν υπολείμματα λιπιδίων και για αυτό το λόγο καλούνται λιποπρωτεΐνες. Οι πρωτεΐνες της μεμβράνης της γλοβουλίνης είναι το μικρότερο κλάσμα των πρωτεϊνών του γάλακτος, περίπου 1.5% επί του συνόλου των πρωτεϊνών. Τα λιπίδια και τα υδρόφοβα αμινοξέα των πρωτεϊνών των μεμβρανών έχουν ως συνέπεια την διοργάνωση του μορίου των τελευταίων κατά τέτοιο τρόπο ώστε τα υδρόφοβα τμήματα τους να προσανατολίζονται προς το λίπος και τα υδρόφιλα τμήματα προς το νερό. Ειδικότερα τα φωσφολιπίδια και τα λιπολυτικά ένζυμα προσροφούνται στη μεμβράνη. Ένζυμα του γάλακτοςΤα ένζυμα που απαντούν στο γάλα προέρχονται από το ζώο από το οποίο παράχθηκε το γάλα και από βακτήρια. Τα πρώτα συγκαταλέγονται στα φυσικά συστατικά του γάλακτος. Τα τελευταία, τα βακτηριακά ένζυμα, ποικίλλουν σε είδος και σε αφθονία και δεν θεωρούνται στο κομμάτι αυτό. Ορισμένα από τα ένζυμα του γάλακτος χρησιμοποιούνται κατά τον ποιοτικό του έλεγχο. Μεταξύ των σημαντικότερων είναι η περοξειδάση, η φωσφατάση και η λιπάση. ΛακτοπεροξειδάσηΗ λακτοπεροξειδάση μεταφέρει οξυγόνο από το υπεροξείδιο του υδρογόνου (H2O2) σε άλλες άμεσα οξειδώσιμες ενώσεις. Το ένζυμο αυτό αδρανοποιείται κατά την θέρμανση του γάλακτος στους 80οC για μερικά δευτερόλεπτα, γεγονός το οποίο βρίσκει εφαρμογή κατά τον έλεγχο της παστερίωσης του γάλακτος. Η απουσία/παρουσία του ενζύμου χρησιμοποιείται ως απόδειξη ότι η θερμοκρασία παστερίωσης έφθασε τους 80oC ή όχι. Αυτή η μέθοδος ελέγχου της παστερίωσης είναι γνωστή ως το τεστ περοξειδάσης του Storch. ΦωσφατάσηΗ φωσφατάση έχει την ιδιότητα να διασπά ορισμένους εστέρες του φωσφορικού οξέος σε φωσφορικό οξύ και την αντίστοιχη αλκοόλη. Η παρουσία της φωσφατάσης στο γάλα μπορεί να ανιχνευτεί με την προσθήκη ενός εστέρα του φωσφορικού οξέος και ενός αντιδραστηρίου που οδηγεί σε αλλαγή του χρώματος αντιδρώντας με την αλκοόλη που απελευθερώνεται. Η αλλαγή του χρώματος αποδεικνύει την παρουσία φωσφατάσης. Η φωσφατάση καταστρέφεται κατά την συνήθη παστερίωση του γάλακτος (72οC για 15-20 δευτερόλεπτα), επομένως το τεστ της φωσφατάσης μπορεί να χρησιμοποιηθεί για την επιβεβαίωση ότι επιτεύχθηκε η επιθυμητή θερμοκρασία κατά την παστερίωση. ΛιπάσηΗ λιπάση διασπά το λίπος σε γλυκερόλη και λιπαρά οξέα. Η περίσσεια ελεύθερων λιπαρών οξέων στο γάλα και τα γαλακτοκομικά προϊόντα οδηγεί σε ταγγή γεύση. Η δράση του ενζύμου αυτού φαίνεται στις περισσότερες περιπτώσεις να είναι αδύναμη, αν και το γάλα ορισμένων ζώων χαρακτηρίζεται από έντονη δραστηριότητα λιπάσης. Η ποσότητα της λιπάσης στο γάλα πιστεύεται ότι αυξάνει προς το τέλος του γαλακτοπαραγωγικού κύκλου. Καμιά αντίδραση δεν λαμβάνει χώρα μεταξύ της λιπάσης του γάλακτος και των λιποσφαιρίων εφόσον η μεμβράνη των τελευταίων παραμένει άθικτη. Με την καταστροφή όμως της μεμβράνης των λιποσφαιρίων η λιπάση βρίσκει υπόστρωμα με αποτέλεσμα το σχηματισμό ελεύθερων λιπαρών οξέων. Όταν το γάλα αντλείται κρύο με ελαττωματική αντλία, ή μετά από ομογενοποίηση του κρύο χωρίς να έχει προηγηθεί παστερίωση σχηματίζονται ελεύθερα λιπαρά οξέα. Τα λιπαρά οξέα και ορισμένα άλλα προϊόντα της ενζυματικής αυτής αντίδρασης προσδίδουν ταγγή γεύση στο προϊόν. Πηγές:
|
|
| ||
| Food-Info.net is an initiative of Stichting Food-Info, The Netherlands | ||||||