Door Marjolijn Schrijnen
Wageningen Universiteit, Literatuuronderzoek
SAMENVATTING 5
H1. INLEIDING 6
H2. GESCHIEDENIS VAN DE DETECTIE VAN HET CALICIVIRUS 7
H3. CALICIVIRIDAE FAMILIE 8
3.1 CLASSIFICATIE 8
3.2 MOLECUUL EIGENSCHAPPEN 8
H4. GASTRO-ENTERITIS: 9
4.1 ALGEMEEN 9
4.2 ROUTE VAN SLV 10
4.3 SYMPTOMEN EN BEHANDELING 10
H5. DETECTIE 11
5.1 DETECTIE VAN HET VIRUS 11
5.2 VIRUSDETECTIE IN VOEDSEL EN WATER 11
H6. BESMETTINGEN 12
6.1 ALGEMEEN 12
6.2 BESMETTELIJKE PERIODE 12
6.3 BESMETTINGEN ALTIJD EN OVER DE HELE WERELD? 12
6.4 IMMUNITEIT 12
H7. TRANSMISSIE VAN HET HUMAN CALICIVIRUS 13
7.1 TRANSMISSIE ROUTES 13
7.1.1 Mens-naar-mens 13
7.1.2 Voedselbesmetting 13
7.1.2.1 Besmette schelpdieren 14
7.1.2.2 Besmet voedsel door geïnfecteerd voedselhandelaren 14
7.1.2.3 Fruit /groente besmet door irrigatie of wassen 15
7.1.3 Transmissie via besmet water 15
7.2 ZOÖNOSE TRANSMISSIE 15
7.3 TRANSMISSIE IN ZIEKENHUIZEN EN VERPLEEGTEHUIZEN 15
7.4 ANDERE VORMEN VAN EXPLOSIE VEROORZAKERS 16
H8. PREVENTIE 17
8.1 DESINFECTIE 17
8.2 ALGEMENE PREVENTIEVE MAATREGELEN 17
H9. GEVOLGEN VAN EEN EXPLOSIE MINIMALISEREN 18
9.1 MAATREGELEN TEN AANZIEN VAN PATIËNTENEN CONTACTEN 18
9.2 WERING VAN WERK, SCHOOL OF KINDERDAGVERBLIJF 18
9.3 OVERIGE ACTIVITEITEN 18
9.3.1 Meldingsplicht 18
9.3.2 Inschakelen van andere instanties 18
H10. CONCLUSIE EN DISCUSSIE 19
LITERATUURLIJST 20
Samenvatting
Virussen lijken steeds meer in de belangstelling komen te staan als veroorzakers van voedselinfecties. In dit onderzoek zal specifiek gekeken worden naar het SLV (Sapporo Like Virus).
Het Sapporo virus is als eerste ontdekt in 1977 tijdens een gastro-enteritis uitbreek in een kindertehuis in Sapporo, Japan. Dit ontdekte virus behoort tot de familie Caliciviridae. Deze familie is onderverdeeld in Vesivirus, Lagovirus, Norwalk Like Virus en Sapporo Like Virus. De laatste twee virussen behoren samen tot de humane enterale Calicivirussen (HuCVs), maar verschillen wel in epidemiologie. HuCVs bevatten 1 molecuul van lineair positief strengs RNA en hebben een diameter van 27-40 nanometer. De virussen hebben geen envelop en zijn icosaëder.
In Nederland worden jaarlijks zo'n 4,5 miljoen mensen getroffen door gastro-enteritis. Circa 5% van de gevallen van gastro-enteritis in Nederland waarvoor een huisarts wordt geconsulteerd, wordt veroorzaakt door SLV. Dit virus is een belangrijke oorzaak van 'sporadische' gevallen van gastro-enteritis en wordt ook wel winter vomiting disease' genoemd.
Het Sapporo Like Virus heeft, in vergelijking met die van bacteriën, een zeer kleine infectieuze dosis (10-100 virusdeeltjes) en een incubatietijd van één tot drie dagen. Het SLV wordt door de mens opgenomen via de orale route, waarna de meest voorkomende klinische symptomen misselijkheid, braken, hoofdpijn, buikpijn, diarree en milde koorts zijn. Het begin van de ziekte is abrupt, normaal binnen 24-28 uur na blootstelling aan het virus en de duur van de ziekte is relatief kort (12-60 uur).
Een diagnose van het virus kan gesteld worden met behulp van elektronenmicroscopie, moleculair biologische methoden (RT-PCR) en sequentieanalyse.
Geïnfecteerde personen ontwikkelen enige immuniteit, daarnaast is er momenteel nog geen vaccin tegen de gastro-enteritis besmetting ontwikkeld.
Explosies van het virus kunnen zich verspreiden via mens-naar-mens contact, voedselbesmetting en waterbesmetting routes. Een gevaarlijke plaats waar vaak transmissie op treedt is in ziekenhuizen, hier kunnen zowel patiënten als personeel beschadigd worden. Of bij dit virus ook sprake is van zoönose transmissie wordt onderzocht.
De besmetting met het Sapporo Like Virus is meestal fecaal-oraal, maar aërogene transmissie via braaksel speelt ook een belangrijke rol. Naast deze vormen van transmissie zijn er nog andere explosie veroorzakers.
Calicivirussen zijn resistent tegen vele desinfecteermiddelen in de gebruikelijke dosering en tegen sterke schommelingen in de pH. Maar het exacte effect van desinfectantia op Calicivirussen is nauwelijks onderzocht omdat ze niet kweekbaar zijn en er geen diermodel van is.
Naast preventiemaatregelen en maatregelen voor personen die besmet zijn, gelden ook regels voor meldingsplicht.
H1. Inleiding
Voedsel is één van de primaire behoeften van de mens. Het is dan ook zaak dat het voedsel dat men gebruikt veilig en vrij van pathogene micro-organismen is. Naast pathogene micro-organismen kunnen ook virussen bederf veroorzaken. Virussen lijken steeds meer in de belangstelling komen te staan als veroorzakers van voedselinfecties. In dit onderzoek zal specifiek gekeken worden naar het SLV (Sapporo Like Virus), welke een belangrijke soort virus is op dit gebied. De ernst van dit virus zal bepaald worden, de risico's voor de consument en welke producten risico lopen om besmet te worden met dit virus. Ook de preventie van besmettingen met het virus is een belangrijk aspect wat behandeld zal worden.
Dit onderzoek is geheel gebaseerd op literatuurstudie.
H2. Geschiedenis van de detectie van het Calicivirus
In 1972 werd in fecesmonsters, welke verzameld waren tijdens een epidemie van gastro-enteritis op een basisschool in Norwalk, voor het eerst het Calicivirus door middel van elektronenmicroscopie aangetoond. In de jaren daarna zijn ook andere virussen geïdentificeerd en genoemd naar de plaats waar ze gevonden waren (bijvoorbeeld Hawaï en Sapporo). [1]
Het Sapporo virus, of human Calicivirus Sapporo, met typische oppervlakte morfologie was als eerste ontdekt in 1977 tijdens een gastro-enteritis explosie in een kindertehuis in Sapporo, Japan. Een explosie is een incident waarbij twee of meer personen die hetzelfde gegeten of gedronken hebben, na dezelfde tijd ziek worden met dezelfde ziekteverschijnselen. [10] Het tehuis waar de explosie was had 93 bewoners van 1 tot 27 maanden oud. Van deze kinderen hadden 77 (83%) gastro-intestinale symptomen, daarvan had 95% diarree, moest 44% overgeven en had 18% koorts. Het huis heeft 4 gescheiden kamers, waarin de kinderen per leeftijdsgroep huisden. De explosie bewoog zich in opéénvolging van kamer naar kamer, waarschijnlijk door persoon- naar- persoon spreiding. Van deze kinderen zijn 61 monsters onderzocht, hieruit bleek dat 48% Calicivirus deeltjes bevatten. Een relatie tussen het aantonen van virus in de feces en de dag ziekte was goed aangetoond. [2]
Sinds die tijd zijn, morfologische en antigeen gelijkende virussen frequent gedetecteerd in hetzelfde instituut, in associatie met gastro-enteritis explosies.
In het begin was het Calicivirus alleen gevonden bij zwijn, verschillend wild en huisdieren. De studie van deze virussen was dan ook alleen gericht op het gebied van de veterinaire medicijnen. In 1976, direct na de introductie van de elektronen microscoop, zijn in de stoelgang van kinderen morfologisch gezien typische Calicivirussen van menselijke oorsprong gevonden.
De jaren daarna, werden sporadische explosies van gastro-enteritis, welke geassocieerd konden worden met de morfologische typische Calicivirus, in vele landen gerapporteerd. Studies naar gastro-enteritis in Londen en Sapporo hebben overtuigend bewijs dat deze virussen gastro-enteritis kunnen veroorzaken bij mensen van elke leeftijd. [2]
H3. Caliciviridae familie
3.1 Classificatie
Begin jaren 90 zijn moleculaire technieken ontwikkeld waarmee nadere typering van de virussen en indeling in genera kon plaatsvinden. De familie Caliciviridae in dieren en mensen is onderverdeeld in 4 generaties:
Vesivirus (zwijn)
Lagovirus (konijn)
Norwalk Like Virus (ook wel bekend als small-round-structured-virussesof SRSV):
GI (prototype) en
GII (Snow Mountain Virus),
deze twee groepen zijn weer verder verdeeld tot vele clusters op basis van
verschil in opeenvolging van het RNA afhankelijke RNA-polymerase en
ingekapselde eiwit gebieden van de genomen.
Sapporo Like Virus (klassieke Calicivirussen):
Sapporo virus 82, prototype, genogroup I (o.a. Manchester en Houston virus),
London 92 genogroep II (Pretoria 92/94) en
Parkville virus genogroep III (Houston 90).
De eerste twee genera veroorzaken in principe alleen veterinaire infecties.
Belangrijk voor de mens zijn het Norwalk Like Virus en het Sapporo Like Virus, samen behoren deze virussen tot de humane enterale Calicivirussen (HuCVs). Calicivirussen zijn de verwekkers van het merendeel van de niet-bacteriële gastro-enteritisden (zowel wat betreft epidemieën als sporadische gevallen). Binnen de Calicivirussen wordt een grote verscheidenheid aan virustypes gevonden die onderling sterk verschillen wat betreft de samenstelling van de viruseiwitten.
De meeste gastro-enteritis explosies worden veroorzaakt door virussen behorend tot de familie Caliciviridae en specifiek het genus Norwalk Like Virus. Gebaseerd op morfologie, genome volgorde en organisatie zijn SLV en NLV in verschillende genera onderverdeeld. De twee groepen verschillen tevens in epidemiologie: de NLVs veroorzaken klachten bij personen van alle leeftijden, terwijl de SLVs vooral ziekteverschijnselen veroorzaken bij zuigelingen en kinderen. [1][2][3]
3.2 Molecuul eigenschappen
HuCVs bevatten 1 molecuul van lineair positief strengs RNA en het virus is 27-40 nanometer in de diameter. De virussen hebben geen envelop en zijn icosaëder. Een icosaëder is een normaal veelvlak met 20 gelijke driehoekige vlakken en 12 hoeken. De naam Calicivirus is afkomstig van de Latijnse calyx, wat kelk of beker betekent, en verwijst naar de bekervormige depressie in sommige strengen. Het Sapporo virus heeft een typische David ster' configuratie. [2][3][4][5][6]
H4. Gastro-enteritis:
4.1 Algemeen
Gastro-enteritis is de meest voorkomende en in de volksgezondheid de meest belangrijke ziekte bij mensen. In Nederland worden jaarlijks zo'n 4,5 miljoen mensen getroffen door deze maagdarmkanaal infectie. Deze ontsteking van het maagdarmkanaal kan veroorzaakt worden door een scala aan virussen, bacteriën en parasieten. [7] Circa 5% van de gevallen van gastro-enteritis in Nederland waarvoor een huisarts wordt geconsulteerd, wordt veroorzaakt door SLV(ter vergelijking: 3,9% Salmonella, 10,5% Campylobacter als veroorzakers van gastro-enteritis). [5] In figuur 1 is te zien welk deel van de onderzochte explosies door welk specifiek virus wordt veroorzaakt. [1]
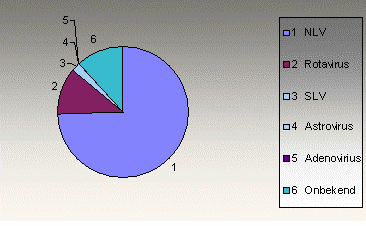
Figuur 1. Oorzaken van onderzochte explosies.
Het percentage SLV infecties in Nederland is 6% per 1000 mensen per jaar en in Engeland is het percentage 0.01% per 1000 mensen per jaar. [6]
Gedurende de eerste vijf levensjaren zal elk kind te maken krijgen met ziekte welke diarree tot gevolg heeft. Hierbij komen risico's van uitdroging en voedseldeficiëntie kijken. Vooral in ontwikkelingslanden lijden veel kinderen aan gastro-enteritis. Deze aandoening is voor 25-30% de doodsoorzaak bij kinderen onder de vijf jaar.
In meer ontwikkelde landen is sterfte door gastro-enteritis zeldzaam, maar het is wel een belangrijke oorzaak van ziekte en economische kosten.
Moderne methoden van voedseldistributie zorgen voor grote, diffuse en transnationale explosies. Hetzelfde geldt voor besmet drinkwater. Het grootste volksgezondheidsimpact is bij explosies op gezondheidszorg gebied. [6]
4.2 Route van SLV
Het SLV wordt opgenomen door de mens via de orale route. Als zuur- stabiele virussen passeren ze de maag en vindt in de dunne darm vind replicatie plaats.
Licht en elektronen microscopie laten zien dat individuen met deze klinische ziekte aandoeningen aan de dunne darm krijgen. Het mucosa slijmvlies raakt ontstoken en absorptie epitheelcellen ontwikkelen een abnormale gedaante. Ook kan afstomping van de villi, verkorting van de microvilli, uitzetting van het endoplastisch reticulum, opgezwollen mitochondria en intracellulaire oedeem microscopisch waargenomen worden. Wel keert de dunne darm binnen twee weken weer terug tot een normale gedaante. Deze waarnemingen zijn gedaan bij gezonde vrijwilligers, dus hoe dit virus werkt bij ouderen, zieken of kinderen blijft onduidelijk. [6]
4.3 Symptomen en behandeling
De meest voorkomende klinische symptomen zijn misselijkheid, braken, hoofdpijn, buikpijn, diarree en milde koorts. Er is geen bloed- of slijmbijmenging in de feces. Het begin van de ziekte is abrupt, normaal binnen 24-28 uur na blootstelling en de duur van de ziekte is relatief kort (12-60 uur) bij mensen met een goede gezondheid, soms is de duur bij ouderen aanzienlijk langer. Infecties van SLV zijn mild en zelf- beperkend en vereisen daardoor geen medische aandacht. Toch is het risico van uitdroging door braken en /of diarree hoger bij ouderen en kleine kinderen en zal bij deze groep wel medische hulp nodig kunnen zijn. Sterfte in associatie met Calicivirus infectie is beschreven, maar de causaliteit is formeel niet bewezen. [5][6]
Bij vertoning van deze gastro-enteritis symptomen kan een persoon behandeld worden. De symptomatische behandeling is gericht op het voorkomen/ bestrijden van uitdrogingsverschijnselen (vochttoediening). [5]
H5. Detectie
5.1 Detectie van het virus
Bij een infectie met gastro-enteritis virussen wordt normaliter een diagnose gesteld door de detectie van de pathogenen in feces monsters van zieke mensen, in plaats van het meten van antilichamen response in serum. Vroeger werden van virussen diagnoses gesteld door een suspensie van een feces monster te scannen onder een elektronen microscoop. Een diagnose van Sapporo Like Virussen kan worden gesteld door detectie van viraal nucleine zuur met behulp van reverse transcriptase polymerase chain reaction (RT-PCR). Het probleem bij PCR is dat ook de kleine stukjes virus worden aangetoond. Twee personen kunnen dezelfde hoeveelheid virussen in hun lichaam hebben maar verschillen van reactie, dus de ene wel besmet en de andere niet. Bij zo'n diagnose kan dus alleen de eventuele aanwezigheid van het virus worden vastgesteld en bevat de diagnose geen toegevoegde informatie welke kan helpen bij de bepaling of de persoon een risicofactor kan zijn in de voedselketen. Aan de andere kant is de minimale infectueuze dosis bij deze virussen zo laag dat elke geïnfecteerde persoon de ziekte kan verspreiden. Sapporo Like Virussen kunnen in klinische samples m.b.v. stoelgang, genome detectie en elektronen microscopie worden aangetoond. [8]
Een diagnose kan dus gesteld worden met behulp van elektronenmicroscopie of met behulp van moleculair biologische methoden, reverse transcriptase PCR. Deze methoden zijn echter niet voor routinematige diagnostiek beschikbaar. Virussen uit feces kunnen ook getypeerd worden door middel van sequentieanalyse. Daarmee is het mogelijk om aanwijzingen te krijgen voor een gezamenlijke bron van infectie. Door middel van deze technieken zijn in de Verenigde Staten en Europa voedselgerelateerde explosies van gastro-enteritis uit verschillende geografische gebieden aan elkaar gekoppeld. Inmiddels zijn snellere typeringstechnieken ontwikkeld (op basis van probe-hybridisatie door middel van een reverse-line blotting assay), die meer algemeen gebruikt zouden kunnen worden. [5]
5.2 Virusdetectie in voedsel en water
Moleculaire methoden zijn beschreven en gebruikt voor het aantonen van Calicivirus in voedsel of water. Deze zijn echter in Nederland niet beschikbaar voor routinematige bepalingen. Het aantonen van indicatororganismen voor fecale verontreiniging op verdacht voedsel of in water blijkt ongeschikt te zijn voor deze virussen. Bovendien is volstrekt onbekend wat de gevoeligheid is van de beschikbare detectiemethoden, met name bij ongelijkmatig besmette partijenvoedsel. Als Calicivirus in voedsel wordt aangetroffen, is het mogelijk om door middel van typering een nauwkeurigere beschrijving van het virus te krijgen. Dit kan gebruikt worden om transmissiewegen in kaart te brengen. Deze technieken zijn in diagnostische laboratoria niet operationeel. De huidige detectie methode van dit virus in water en in voedsel welke wel operationeel is, is het gebruik van de genome detectie methode. [5]
H6. Besmettingen
6.1 Algemeen
De Calicivirussen zijn zeer besmettelijk. Een belangrijke handicap in het onderzoek is dat de virussen niet in vitro te kweken zijn. Daardoor is het bijvoorbeeld niet mogelijk om de besmettelijkheid van virus bevattende preparaten te bepalen, derhalve door experimenten met vrijwilligers. Er wordt gesproken van een zeer kleine infectieuze dosis (10-100 virusdeeltjes). Deze infectieuze dosis is erg laag in vergelijking met de minimale infectieuze dosis van bijvoorbeeld bacteriën. Bij bacteriën zijn meestal meer dan 10 4 cellen nodig om ziek te worden (Salmonella 10 6, Clostridium 10 8 cellen). [9] De incubatietijd is één tot drie dagen. Circa 45% van de personen die zijn blootgesteld aan Calicivirussen wordt daadwerkelijk ziek. De Calicivirussen zijn zeer besmettelijk en secundaire infecties komen dan ook vaak voor.
Niet alle gevallen van Calicivirus infecties doen zich voor tijdens explosies: SLVs zijn een belangrijke oorzaak van 'sporadische' gevallen van gastro-enteritis. [5]
6.2 Besmettelijke periode
Infectieuze virusdeeltjes kunnen in de ontlasting worden aangetoond niet alleen tijdens de periode van klachten, maar ook enkele dagen vóór en mogelijk tot ongeveer tien dagen na de ziekteverschijnselen. Het is vooralsnog onduidelijk hoe lang na klinisch herstel het virus nog is over te dragen. Een explosie door overdracht van het virus langer dan 48 uur na klinisch herstel is in de literatuur slechts één keer beschreven. Onderzoekscentra kunnen bij 30% van de mensen met klachten tot vier weken daarna nog virus RNA in de ontlasting aantonen. [5]
6.3 Besmettingen altijd en over de hele wereld?
Epidemieën, maar ook sporadische gevallen van gastro-enteritis veroorzaakt door het SLV komen wereldwijd voor. Infecties door Calicivirus worden het hele jaar door gezien, maar zijn toch enigszins seizoensgebonden. De piek ligt namelijk in de wintermaanden ('winter vomiting disease'). In Europa begint het virus vooral op te steken in oktober en november, de piek in januari en de aftakeling begint in mei of juni. [6]
6.4 Immuniteit
Uit onderzoek blijkt dat bij sommige mensen wel darm ontstekingen worden ontdekt maar geen symptomen van ziekte. Geïnfecteerde personen ontwikkelen immuniteit, maar deze is kortdurend en voornamelijk type specifiek. Praktisch gezien kan een persoon dus achtereenvolgens door verschillende type Calicivirussen geïnfecteerd worden wat grotendeels de hoge incidentie van infecties verklaart. [1][5][6]
Momenteel is er geen vaccin tegen de gastro-enteritis besmetting. Een universele vaccinatie is onnodig, maar een vaccin dat een korte termijn immuniteit tijdens explosies biedt zou bruikbaar zijn. Dit is handig voor de ouderen in verzorgingstehuizen en andere individuen met een slecht immuunsysteem.
Onderzoek wordt onder andere gedaan naar VLPs. VLP's zijn Virus Like Particels, deze zijn morfologisch en antigeen gelijkend aan levensvatbare virus deeltjes. Deze niet vermeerderende immunogenen zorgt voor een immune respons in experimenten met dieren en zijn kandidaten voor een menselijk vaccin. [3]
H7. Transmissie van het humane Calicivirus
7.1 Transmissie routes
De explosies van het virus worden veroorzaakt door mens-naar-mens contact, voedselbesmetting en waterbesmetting routes. In de afgelopen jaren is ook de rol van milieu besmetting en besmetting van onbewerkt fruit en groente aangetoond. [6]De besmetting is meestal fecaal-oraal, maar aërogene transmissie via braaksel speelt ook een belangrijke rol. De kans op transmissie bij braken is mogelijk groter dan bij diarree. [5]
Explosies zijn meestal het resultaat van meer dan één vorm van transmissie en het is moeilijk om een explosie op één vorm van transmissie af te schuiven. Een explosie kan begonnen worden door één vorm, maar de meerderheid van de infecties kan veroorzaakt zijn door een andere vorm van transmissie. Zie figuur 2.
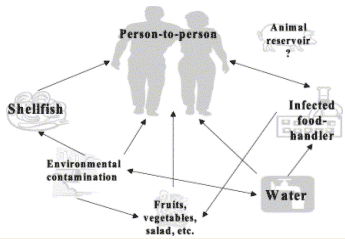
Figuur 2. In deze figuur zijn transmissie routes van het humane Calicivirus te zien. Een grote afbeelding van de personen is om te laten zien dat zij een belangrijke rol bij de verspreiding van het virus spelen. [6]
7.1.1 Mens-naar-mens
Verspreiding door mens-naar-mens contact is het meest voorkomend. Geïnfecteerde deeltjes kunnen via de fecaal-oraal route worden getransporteerd, maar ook blijkt dat transmissie door lucht erg belangrijk is. Respiratoire infectie is nog niet gevonden, dus moet waarschijnlijk het aërosole virus worden ingeslikt na inhalatie, wil infectie van de darm optreden. [6]
7.1.2 Voedselbesmetting
De mate van belangrijkheid van transmissie van het virus door voedselbesmetting verschil per land. Voedselbesmettingen zijn wel een belangrijke vorm van transmissie omdat de moderne voedseldistributie virussen toestaat een wijde populatie te bereiken. Drie vormen van voedselbesmettingen zijn typisch namelijk: besmette schelpdieren, besmet voedsel door geïnfecteerd voedselhandelaren en fruit /groente besmet door irrigatie of wassen. [6]
Voedsel kan op verschillende manieren besmet worden. Hier volgt een opsomming van vijf manieren die voedselbesmetting veroorzaken. Ten eerste door contact met (menselijke) feces of fecaal besmet water. Ten tweede door contact met fecaal besmette materiaal (inclusief handen). Ten derde door contact met braaksel of water welke besmet is met braaksel. Ten vierde door contact met milieus waar geïnfecteerde mensen aanwezig waren, ook al is de oppervlakte niet direct besmet met stoelgang of braaksel. En tenslotte door aërosolen welke zijn opgewekt door geïnfecteerde mensen. [6]
In de literatuur worden enkele voedingswaren met name genoemd, maar de achterliggende boodschap is dat al het voedsel, dat is bereid of behandeld door een persoon die het Calicivirus uitscheidt en daarna niet grondig wordt verhit, een mogelijke bron van infectie is. [5]
7.1.2.1 Besmette schelpdieren
Schelpdieren zijn gevaarlijk omdat dit filter-voeders zijn. Het virus groeit niet in de vissen, maar de vissen concentreren de virussen uit besmet afvalwater. De concentratie van de opgenomen virussen blijft voor lange tijd (vier tot zes weken) in infectieuze vorm aanwezig. De organoleptische kwaliteit van de schelpdieren wordt niet aangetast: door proeven en ruiken kan geen onderscheid worden gemaakt tussen besmette en niet besmette schelp- of schaaldieren. [5]
Oester bijvoorbeeld worden rauw of kort gekookt gegeten en veroorzaken hierdoor snel een infectie. Oester monsters worden maandelijks op bacteriële besmetting getest maar niet op virale besmetting. Virussen kunnen ook langer in zee water overleven dan bacteriën. Dus een monster waar geen bacteriën in zijn aangetoond kunnen alsnog wel virussen bevatten. Tevens zijn procedures welke succesvol zijn in het verwijderen van bacteriën, inadequaat in de verwijdering van virussen. [6]
7.1.2.2 Besmet voedsel door geïnfecteerd voedselhandelaren
Voedselhandelaren die in contact komen met mensen die gastro-enteritis hebben, zijn specifieke risico factoren die besmet kunnen worden en zo een bron van virussen worden tijdens het productieproces van voedsel. Zij moeten erop attent zijn dat persoonlijke hygiëne verzekerd moet zijn. Het verhogen van het bewustzijn bij voedselhandelaren over transmissie mogelijkheden van virussen is nodig. De nadruk moet specifiek gelegd worden op stille' transmissie door asymptomisch geïnfecteerde personen en op transmissie via personen die nog steeds het virus bevatten ondanks dat ze al hersteld zijn. Op een twee punten in het HACCP systeem moet goed gelet worden. Ten eerste moet het water, wat gebruikt wordt bij preparatie van het voedsel, van drinkwater kwaliteit zijn. Ten tweede zijn richtlijnen specifiek gericht op de reductie van virale besmetting nodig, omdat het duidelijk is geworden dat huidige indicators voor kwaliteit van water en schelpdieren niet goed genoeg zijn ter preventie van virale besmetting. [8]
Het is duidelijk dat voedselhandelaren een belangrijke oorzaak kunnen zijn van voedselbesmettingen. Op verschillende manieren kunnen de handelaren besmet worden, hier worden er vier genoemd.
(1) Door een geïnfecteerde voedselhandelaar, met symptomen, het verspreiden van het virus gebeurt tijdens de periode van ziekte.
(2) Door een geïnfecteerde voedselhandelaar die herstelt van de ziekte. Verspreiding van het virus kan tot 3 weken na herstel.
(3) Door een geïnfecteerde voedselhandelaar zonder symptomen. Hier vind a- symptomatische infectie plaats, wat vaak voorkomt bij voedselinfectie veroorzakende virussen.
(4) Door voedselhandelaren die contact hebben met zieke personen (zieke kinderen of familie). [8]
Ondanks dat van haast alle explosies de oorzaak ligt bij geïnfecteerde voedsel handelaren, moet ook genoemd worden dat geïnfecteerde personen overal in de keten kunnen voorkomen. [8]
7.1.2.3 Fruit /groente besmet door irrigatie of wassen
Fruit en groenten kunnen worden besmet door hun irrigatiewater, door wassen of bespuiten wat voorafgaat aan vriezen of ze kunnen geïnfecteerd worden door voedselhandelaren die betrokken zijn bij een oogst. [6]
7.1.3 Transmissie via besmet water
Drinkwater kan een explosie van gastro-enteritis veroorzaken in ongeveer elke situatie. Explosies zijn ontstaan als resultante van besmetting van privé waterbronnen als wel grootschalige watersystemen. Voorraden kunnen worden geïnfiltreerd met besmet water in periodes van zware regen val of als vloedstromen optreden.
Ook commercieel gedistribueerd en geproduceerd ijs kan een geografisch wijde explosie veroorzaken, als het water waarvan het ijs gemaakt is geïnfecteerd is. [6]
7.2 Zoönose transmissie
Zoönose transmissie is overdracht van de ziekte van een dier of niet menselijk organisme naar de mens. Het Calicivirus is een belangrijk pathogeen in dieren en mensen. Echter, tientallen niet succesvolle pogingen om dieren en cellijnen te infecteren met het HuCVs suggereren dat SLVs sterk soort gerichte pathogenen zijn. [6]Van enkele groepen virussen in de familie Caliciviridae is aangetoond dat ze een zeer breed gastheer spectrum hebben. [5] Het is nog niet duidelijk of Calicivirussen overdraagbaar zijn tussen dier en mens, omdat er geen bewijs is dat contact met dieren, direct of indirect een bron kan zijn van voedselinfecties. [8]
Bij andere instituten is uit recent onderzoek gebleken dat wel een mogelijkheid van zoönose transmissie bestaat. Transmissie tussen soorten is een zeer zeldzame gebeurtenis en de mogelijkheid van zoönotische spreiding blijft dus onzeker. [6]
7.3 Transmissie in ziekenhuizen en verpleegtehuizen
Om vele redenen zijn Calicivirussen een groot risico voor de gezondheid in ziekenhuizen en verpleegtehuizen. Virussen kunnen geïntroduceerd worden in instituten door voedsel, water of een bezoeker van de communie. En omdat leefruimtes in zowel verpleegtehuizen als ziekenhuizen krap zijn en persoonlijke hygiëne verlaagd is door slechte gezondheid of incontinentie zijn condities uitstekend voor mens-naar-mens transmissie. Aangezien de ziekte ouderen of mensen die al ziek zijn zal treffen, is het HuCV vaak de veroorzaker van erge ziekte of dood in dit soort situaties. Door al deze redenen kunnen grote en uitgerekte explosies, welke moeilijk zijn om te beheersen, in zulke instanties vóórkomen.
De hoge mate van aantasting van typische HuCV explosies beperken zich niet alleen tot de patiënten en ouderen. Ook het personeel kan erg beschadigd worden en bij een explosie zal dan ook 30-50% getroffen worden. Infecties bij het personeel geven problemen in twee opzichten namelijk:
(1) Hun verplaatsingen zorgen voor transmissie naar andere gebieden,
(2) Hun resulterende afwezigheid op het werk zorgt voor personeel te kort en economische verliezen. [6]
7.4 Andere vormen van explosie veroorzakers:
Naast voorspelbare oppervlakten als het tapijt en de wc bril zijn ook oppervlakten als tafels, licht knopjes en jasdelen detecteerbare niveaus met virussen op hun oppervlak. [6]
H8. Preventie
8.1 Desinfectie
Calicivirussen zijn zeer goed in staat om buiten de gastheer te overleven. Zij zijn resistent tegen vele desinfecteermiddelen in de gebruikelijke dosering en tegen sterke schommelingen in de pH. Het effect van desinfectantia op Calicivirussen is nauwelijks onderzocht omdat ze niet kweekbaar zijn en er geen diermodel is. Uit vrijwilligers experimenten in de tachtigerjaren is gebleken dat deze virussen infectieus blijven na blootstelling aan lage pH waarden (pH 2.7), extractie met ether, en behandeling met 3.75-6.25 mg chloor per liter (concentratie vrije chloorionen 0,5-1 mg per liter). Deze hoeveelheden chloor werden gebruikt bij drinkwater desinfectie. Hogere concentraties chloor (10 mg per liter) zorgden wel voor desinfectie. Uit deze experimenten zou ook gebleken zijn dat Calicivirussen resistent zijn tegen verhitting tot 60°C gedurende 30 minuten, maar deze resultaten worden betwijfeld. Door het ontbreken van een kweekmodel is het echter nog niet mogelijk om meer exacte en kwantitatieve data te verkrijgen. Ook is er weinig kennis over het overleven van de Calicivirussen in het milieu, omdat deze virussen moeilijk te detecteren zijn in voedsel of water monsters. [5]
8.2 Algemene preventieve maatregelen
Strikte naleving van hygiënemaatregelen is waarschijnlijk de belangrijkste vorm van preventie. Voor de preventie van voedselbesmetting is het ook van belang geen (humaan) fecaal besmet water te gebruiken bij het telen van voedsel. Door de globalisering van de voedselproductie is controle hierop echter niet altijd mogelijk. In sommige landen wordt een stijging van het aantal gerelateerde voedselinfecties veroorzaakt door consumptie van voedsel (bijvoorbeeld vruchten) uit landen met een lagere hygiënestandaard. Of steekproefsgewijs voedselonderzoek hier bij van nut kan zijn is nog niet duidelijk. Wel kunnen voedsel gerelateerde explosies bijvoorbeeld met behulp van het 'rapid alertsystem for food' van de Europese Unie snel gemeld worden. Een probleem hierbij is wel dat binnen de EU de diagnostiek van deze virussen slechts beperkt beschikbaar is. [5]
H9. Gevolgen van een explosie minimaliseren
9.1 Maatregelen ten aanzien van patiëntenen contacten
Bij een geïsoleerd geval, indien de persoon niet werkzaam is in de voedselbereiding of patiëntenzorg, zijn geen bijzondere maatregelen nodig. Bij een cluster moeten de hygiënemaatregelen aangescherpt worden en moet men de bron proberen te achterhalen indien resten van verdacht voedsel bewaard zijn. [5]
9.2 Wering van werk, school of kinderdagverblijf
Personen die betrokken zijn bij de voedselbereiding of patiëntenzorg in instellingen moeten, vanwege de lage infectieuze dosis, gedurende de ziekteperiode en tot 48-72 uur na klinisch herstel (dus geen braken en/ of diarree meer) andere werkzaamheden verrichten. De hand- en toilethygiëne dient te worden benadrukt bij hervatting van de werkzaamheden. Het weren van kinderen van scholen en kinderdagverblijven is vanuit volksgezondheidsperspectief niet zinvol. [5]
9.3 Overige activiteiten
9.3.1 Meldingsplicht
Volgens de Infectieziektewet zijn voedselinfecties (ook indien veroorzaakt door Calicivirus) meldingsplichtig indien voorkomend bij een persoon werkzaam in de levensmiddelen- of horecasector dan wel beroepsmatig betrokken bij de behandeling, verpleging of verzorging van andere personen. Ook voedselinfecties bij twee of meer personen waarbij de symptomen een verband hebben met het gebruik van verdacht voedsel of vocht zijn meldingsplichtig. Instellingen waar voor infectieziekten kwetsbare populaties verblijven, dienen meerdere gevallen van gastro-enteritis te melden bij de GGD. [5]
9.3.2 Inschakelen van andere instanties
In overleg kan materiaal (feces) afkomstig van patiënten worden onderzocht. Over het algemeen kan men volstaan met vijf ontlastingsmonsters per cluster. Als er pas materiaal ingestuurd kan worden na het verdwijnen van de klachten zullen van meer mensen monsters moeten worden verzameld (omstreeks tien). Bij verdenking op overdracht via besmetvoedsel moet de Keuringsdienst van Waren ingeschakeld worden. [5]
H10. Conclusie en Discussie
Het Sapporo Like Virus veroorzaakt vooral ziekteverschijnselen bij kinderen en zuigelingen. Van de gevallen van gastro-enteritis wordt 5% veroorzaakt door SLV, dit zijn vooral sporadische gevallen.
Geïnfecteerde personen ontwikkelen korte durende en type specifieke immuniteit. Naast deze soort van immuniteit bestaat er nog geen vaccin. Wel is veel onderzoek gaande en worden misschien Virus Like Particels het nieuwe vaccin. Het onderzoek aan SLV kan het beste gebeuren met behulp van sequentieanalyse.
Besmettingen door het virus treden vooral op via mens- naar- mens transmissie, maar ook zijn schelpdieren, groente en fruit, water en voedsel geïnfecteerd door voedselhandelaren belangrijke besmettingsroutes.
Een belangrijke vorm van preventie is strikte naleving van hygiëne maatregelen. Naast preventie kan men verdere verspreiding van gastro-enteritis voorkomen door maatregelen te treffen bij niet geïsoleerde, met het virus besmette, personen.
Het is duidelijk geworden dat SLV een gastro-enteritis veroorzaker is. Door het lage percentage SLV wat de maagdarmkanaal ziekte veroorzaakt is, het de vraag hoe groot de ernst van het virus is.
Men is er nog niet over uit of voedsel voor de SLVs nou ook echt een belangrijke vector is. Waarschijnlijk is mens-naar-mens transmissie wel belangrijk, maar ook speelt transmissie via oppervlaktes en gebruiksvoorwerpen een grote rol. Dat zo weinig SLV aan voedselgerelateerde explosies te relateren is, betekend misschien wel dat het virus wat minder stabiel is "in de keuken" en misschien toch wat verschilt van de NLVs ook al geven ze grotendeels hetzelfde ziektebeeld en lijken ze ook genetisch op elkaar. [10]
Meer onderzoek is dus nog nodig, naar de verschillende vormen waarop SLV geïnactiveerd kan worden, om zo besmetting te voorkomen.
Ook is het misschien van belang om de verschillen tussen SLV en NLV aan te tonen, om onder andere meer inzicht te krijgen in de familie van Caliciviridae.
En als laatste zou meer onderzoek verricht kunnen worden naar het SLV om de ernst van het virus te bepalen.
Literatuurlijst
[1]Vennema H, Vinje J, Wilbrink B, Koopmans M (2001) Overzicht van onderzoek van
virale gastro-enteritis in het jaar 2000 in Nederland. Infectieziekten Bulletin 12, 2
[2]Chiba S, Nakata S, Numata-Kinoshita K, Honma S (2000) Sapporo Virus: History and
Recent Findings. The Journal of Infectious Diseases 181:S303-S308
[3] www.ce.berkeley.edu/~nelson/ce210a/calicivirus/pathogen.htm (10/30/2002)
[4]Prescott L, Harley J, Klein D (1999) Microbiology, 4 th edn. McGraw-Hill, USA
[5] www.lci.lcr.nl/protocollen/calicivirus/lci_cali.pdf (10/30/2002)
[6]Lopman BA, Brown DW, Koopmans M(2002) Human calicivirus in Europe. Journal
of Clinical Virology 24,3:137-160
[7]Wit, M (2002) Gastro-enteritis in Nederlandse bevolking in kaart gebracht.
Infectieziekten bulletin 13, 1
[8]Koopmans M, Duizer E (2002) Foodborne Viruses: An emerging problem, ILSI
Europe Report Series
[9]Abee T, Beumer R, Giffel te M, Hartemink R, Hazeleger W, Nout R, Rombouts F,
Schoutstra S (1999) Inleiding in de levensmiddelenmicroiologie en hygiene, 2nd
edn. Landbouwuniversiteit Wageningen
[10] Duizer, E (2002) Persoonlijk commentaar (28-11-2002)




